为寻求差别定价优势 药企海外认证提速
- 点击次数:
- 日期:2012-03-10
- 编辑:admin
- 来源:
- 评论:0 条
自8月10日广东省出台《广东省物价局药品差别定价办法(试行)》(下称《办法》),对药品实行差别定价后,在业内引起了不小的轰动,运用价格杠杆鼓励药品研发和技术进步也开始在业内产生效应。
《办法》允许“对于获得国际认证并能够出口的药品制剂,现阶段暂考虑国内加工生产并能够出口到欧盟、美国、日本或澳大利亚市场,且连续出口超过2年的”药品制剂实行差别定价。此举已经使得部分企业加速尝试申请FDA或欧盟等主流市场的认证。
仿制药先行
差别定价在鼓励国内制药企业注重药品质量与创新的同时,也加快了药企走出去的步伐。已获得欧盟cGMP认证的深圳立健药业有限公司总经理欧阳青表示:“公司自身本来的定位就是立足于进入国际主流市场,但差别定价政策的出台会加快企业申请国外认证的步伐。
“差别定价对于一些国内企业来说,尤其是已经获得美国FDA或欧盟认证的企业无疑是一项利好和扶持。”欧阳青表示,“差别定价给予了企业政策上的扶持与引导,引导企业注意提高产品质量,引导一些原来不愿意在质量管理上进行投入的企业加大质量管理投入,以高水平的质量参与国际竞争。
国内仿制药同质化竞争日益严重。一面是国际主流市场的利润诱惑,一面是国内市场的产能过剩与恶性竞争,不少本土仿制药企业已开始把目光转向国际药品主流市场,通过开拓海外市场来扩大市场份额。
中国医药质量管理协会副会长孙新生表示,近两年来,我国赴美和欧盟申请认证的本土企业日渐增多,目前大约有十几家。由于有些仿制药在生产过程中成分比较稳定,标准比较规范,实施起来就比较容易,申请国外认证的企业也主要以生产化学药片剂、胶囊居多。
其中浙江海正通过了欧盟EDQM认证,取得了国际制剂工厂的定点生产权;上海华氏制药旗下的天平制药通过了英国的MHRA固体制剂认证和澳大利亚的TGA水溶剂认证,为英国瓦特公司贴牌生产;无锡凯夫和深圳立健则通过了德国的cGMP认证,以德国公司委托加工厂家的身份进入欧洲。
随着仿制药生产和销售越来越规范化、标准化以及国际化,我国仿制药产业走出去会逐渐增多,孙新生表示。
不可盲目
事实上,申请美国FDA或欧盟的cGMP认证,向国际药品质量管理体系靠拢已成为一种趋势。目前我国新版GMP也在修订中,我国的药品质量管理办法也将更加严格和规范。
中国医药企业管理协会会长于明德表示,差别定价政策会促成一批企业去申请国际主流市场认证,加速国内企业走出去。谁先主动往更高一级的质量标准去靠,谁就先行一步,在国内市场质量要求越来越严格的情况下,提高药品质量标准只是早做与晚做的问题。
孙新生表示,如果我国企业严格执行我国现有的质量管理标准,也基本上能够符合美国FDA的要求。
不久前,我国也出台了《药品技术转让注册管理规定》新规,其中规定,对于一些已获得《进口药品注册证》的品种,其生产技术可以由原进口药品注册申请人转让给境内药品生产企业。
目前国内已有企业达到cGMP的要求,《药品技术转让注册管理规定》的出台,会让这些企业优先获益,获得技术转移的机会,于明德表示。
欧阳青表示,通过把制剂产品持续出口到国外,可以在较短时间内在市场中形成较好的口碑,同时也可以把国外的企业引进国内。
由于国内制药企业不管是在硬件设备上还是在管理软件上都与国外的质量管理体系存在一定的差距,国内企业要想获得国际主流市场的认证,必须加大人力物力的投入。欧阳青说:“公司的制剂产品出口到国际市场是一个比较漫长的过程,如果产品没有进入国际主流市场销售,仅单纯停留在国内出售,其投入和产出就不能平衡,所以企业如果单纯是为了招投标方面有利而盲目走上国外认证的道路,必定会加重企业资金链的负担。”
- 2012-03-10 11:03VC行业定价权回归 双巨头垄断收益亮丽





 这六省被禁止跨省调
这六省被禁止跨省调 2014年全国执业兽医
2014年全国执业兽医 广东省动保协会组织
广东省动保协会组织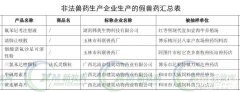 农业部2016年第八批
农业部2016年第八批